대웅제약, 췌장염 치료제 ‘호이스타정’ 임상 3상 허가
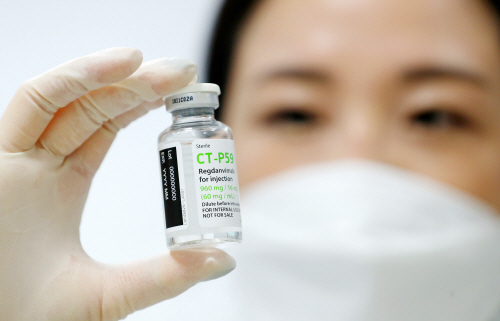
[매일일보 한종훈 기자] 국산 신종 코로나바이러스 감염증(코로나19) 치료제가 임상 결과 발표 및 3상 시험을 앞두고 있어 개발 속도에 불이 붙고 있다.
5일 제약·바이오 업계에 따르면 셀트리온은 이달 13일 대한약학회가 주최하는 하이원 신약개발 심포지아에서 코로나19 항체치료제 렉키로나주의 글로벌 임상 2상 결과를 발표한다.
렉키로나주는 코로나19 완치자의 혈액에 존재하는 중화항체를 선별해 만든 항체치료제다. 경증부터 중등증 수준의 코로나19 환자에 약 90분간 정맥투여 하는 주사제다.
임상 2상은 한국을 비롯해 루마니아, 스페인, 미국에서 총 327명의 경증 및 중등증 코로나19 환자를 대상으로 진행됐다. 셀트리온은 국제 학회에서도 렉키로나주의 임상 2상 결과를 조만간 발표할 계획이다.
앞서 셀트리온은 렉키로나주의 글로벌 임상 2상을 완료한 후 식품의약품안전처(식약처)에 조건부 허가를 신청했다.
이는 코로나19 치료제에 국민의 관심이 집중된 점을 고려한 식약처의 요청으로 별도의 지침이 있을 때까지 상세한 데이터를 비공개하기로 합의했다. 하지만 명확한 임상 결과는 오리무중이라는 우려가 확산하자 조기에 발표하기로 결정했다.
셀트리온은 조건부 허가와 별개로 전 세계 10여개 국가에서 코로나19 항체치료제의 임상 3상에도 돌입할 예정이다.
최근 식약처는 중증 코로나19 환자를 대상으로 대웅제약 호이스타정과 길리어드사이언스 렘데시비르를 병용해 효과를 확인하는 임상 3상 시험도 승인했다. 호이스타정은 만성 췌장염 등에 쓰는 전문의약품으로 먹는 형태의 코로나19 치료제로 개발 중이다.
앞서 호이스타정은 경증 코로나19 환자에 투여한 임상 2a상 중간 결과에서 통계적 유의성을 달성하는데 실패했다. 대웅제약은 “코로나19 환자가 음성으로 전환되는 데 걸리는 시간이 통계적으로 유의하지는 않았으나 바이러스가 제거되는 속도가 위약군에 비해 빨랐다고 주장하며 개발을 이어가겠다”고 밝혔다.
이번 임상시험은 중증 환자를 대상으로 진행할 예정이다. 임상시험 실시기관은 국립중앙의료원으로 목표 대상자 수는 1072명이다. 임상에서 유의미한 결과가 나온다면 코로나19 중증 환자 치료에 도움이 될 것으로 보인다.
이밖에 JW중외제약이 코로나19 치료제로 개발 중인 윈트 표적항암제 후보물질 CWP291이 동물모델에서 항바이러스 효과를 보였다. JW중외제약은 CWP291이 코로나19 체내 수용체 단백질인 GRP78을 억제하는 기전을 바탕으로 코로나19 치료제로 개발할 가능성이 있다고 판단했다.